
JEWELFISH是一项多中心、探索性◆★、非对照开放标签研究,共纳入174例6个月至60岁确诊为5qSMA的患者★◆★,其中有76例既往接受诺西那生治疗,对既往经治的儿童和成人SMA患者◆★■■,予以每日1次口服利司扑兰治疗[2]。
主持国家自然科学基金3项◆◆★■■;浙江省重点研发计划、浙江省自然科学基金等科研项目10余项◆★★■■;以第一或通讯作者发表中英文学术论文40余篇◆◆★◆◆■,其中在SMA领域发表SCI与国内一级核心期刊论文30余篇,申请/授权国家发明专利3项,主持国内多/单中心临床研究7项
该研究共观察了15例转换治疗方案的SMA患者的安全结局,在利司扑兰治疗时长最长达3个月的随访期间,共观察到4例患者出现6例次不良事件◆★,无患者出现实验室结果异常★■◆◆◆★。该研究结果表明,在最后一剂诺西那生治疗后90天内接受利司扑兰治疗安全性良好,这一洗脱期比JEWELFISH研究中的更短■■◆★◆★,为利司扑兰在临床实践中的应用提供了数据支持■★★◆。
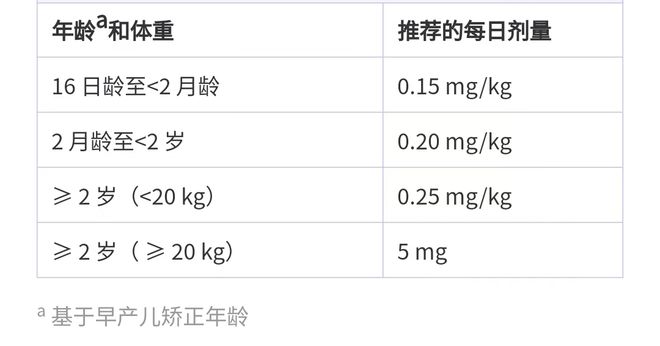
本研究回顾性地收集了既往在浙江大学医学院附属儿童医院接受诺西那生治疗的SMA儿童患者随访数据◆◆■◆★■,这些儿童患者均被诊断为5qSMA,并在最后一次注射诺西那生后的90天内接受利司扑兰治疗★■,按照患者年龄和体重确定给药方案(表1)。
[1] 中华医学会神经病学分会, 中华医学会神经病学分会神经遗传学组■◆■■. 脊髓性肌萎缩症中国三级预防指南[J]■◆. 中华神经科杂志, 2023, 56(5): 476-484.
2007年获浙江大学儿科学博士学位,曾留学美国密歇根大学神经科学研究所从事博士后研究,美国罗马琳达大学附属儿童医院访问学者
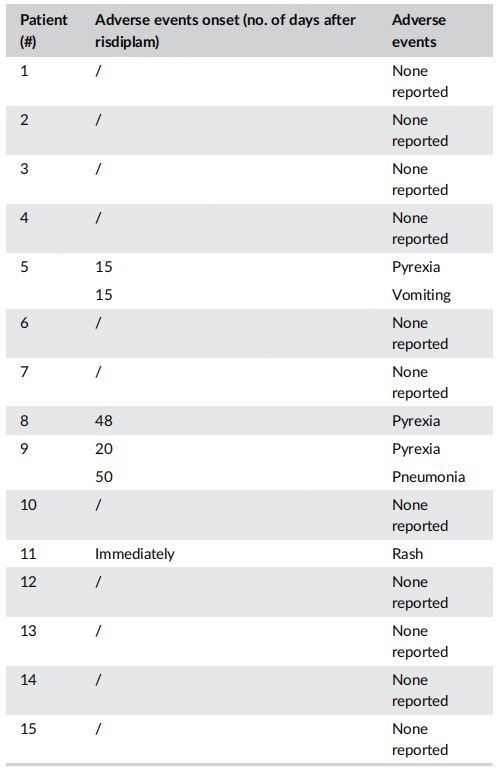
本研究重点收集并分析了利司扑兰的安全性数据■■■◆◆,主要通过与父母进行访谈和实验室检查来获得,包括不良事件、肝功能、肌酐和全血细胞计数■◆◆★★★。该研究最终共纳入15例SMA患者,包括1例SMAⅠ型◆■■★◆■、12例SMAⅡ型和2例SMAⅢ型,患者性别分布较均衡,男女比例为0★■★.86★★:1,患者SMN2基因拷贝数均为3。在症状方面,有3例患者已经出现脊柱侧凸,仅1例可行走。
JEWELFISH研究结果显示[2],接受利司扑兰治疗24个月后,SMA患者的中位SMN蛋白水平较基线倍以上,且与既往接受的治疗无关,并且可独走SMA患者的 6MWT 步行总距离增加,第 24 个月时从第一分钟到最后一分钟(第 6 分钟)步行距离较基线),提示患者的疲劳程度降低★★。JEWELFISH研究中经治患者从诺西那生转换至利司扑兰的洗脱期均在90d及以上◆■◆★,但在真实世界中■★◆◆■★,部分患者会选择在上次给药的半衰期后再进行转换,部分患者可能会选择直接转换,还有部分患者考虑联合用药,本研究旨在探究对于诺西那生疗效不佳且患者病情迅速恶化时加用利司扑兰的时机■◆★,如研究结果所示,对于大部分诺西那生治疗下病情平稳的患者,在短时间内加用利司扑兰的获益是不明确的,并且还存在用药成本的问题,基于上述原因两者联合使用可能并不可取,因此也就有必要对转换治疗过程中的洗脱期进行进一步探索,尤其需要对该过程中的不良事件进行严密监测。
利司扑兰是一种靶向SMN2基因的口服小分子mRNA剪接调节剂,适用于16日龄及以上的SMA患者。此前JEWELFISH研究已表明,既往经治的SMA患者接受利司扑兰治疗12个月的安全性与利司扑兰初治SMA患者中报道的结果一致★■◆■■,这些经治患者在由诺西那生转换至利司扑兰治疗时需经过一段洗脱期(≥90天)[2]。
脊髓性肌萎缩症(SMA)是最常见的婴幼儿常染色体隐性遗传病之一■◆■,主要是运动神经元存活基因1(SMN1)突变导致的脊髓前角运动神经元退行病变,以肌无力和肌萎缩为主要临床表现[1]。迄今为止,全球范围内共有3种疾病修饰治疗药物(DMT)获批用于治疗SMA,已于国内上市的有利司扑兰与诺西那生,由于有多种治疗选择,患者可能会出于多种原因要求转换治疗或联合使用◆■◆◆,因此了解这些药物在序贯或联合使用时的安全性十分有必要。
需要注意的是,本研究仍存在样本量小◆■、数据来自单一中心的局限性,本研究中所有受试者的SMN2拷贝数均为3,临床症状相对较轻,并且样本量小还导致年龄范围并没有完全覆盖利司扑兰的适用人群年龄范围(16日龄及以上),因此未来仍需开展进一步研究★★,纳入SMN2拷贝数、临床表型以及年龄范围更广泛的受试者参与研究,以探索利司扑兰更广泛的转换治疗场景。
近几年,SMA 的DMT药物发展迅速,根据此前临床试验和真实世界研究★◆■★■★,SMA患者在治疗期间需要调整治疗方案的具体原因包括既往治疗不耐受◆★★◆■、疗效不佳,或是因脊柱问题无法接受鞘内注射、患者和照护者用药偏好,以及特殊原因需要居家治疗等[2]★★★■■。
在安全性方面,JEWELFISH研究最常见的不良事件依次是发热、上呼吸道感染■◆■、头痛、恶心、腹泻、鼻咽炎和呕吐,而本项研究中常见的不良事件为发热,尚未出现鼻咽炎★★◆◆、腹泻、头痛或其他情况◆★;JEWELFISH中最常见的严重不良反应是肺炎,在本项研究观察期间只发生过一次。这表明,在最后一次诺西那生治疗后的90天内接受利司扑兰并没有导致另外的严重程度或不良事件。此外,从实验室结果来看,短期接受利司扑兰治疗后患者没有发现实验室指标异常■◆,这表明诺西那生短期内接受利司扑兰治疗对儿童肝肾功能没有不利影响。
近期,浙江大学医学院附属儿童医院毛姗姗教授团队在《Muscle & Nerve》上发布了一项研究,表明在接受诺西那生治疗后90天的洗脱期内再接受利司扑兰治疗时安全性仍然良好[3],该研究是对JEWELFISH研究的进一步补充。本文现撷取该研究精华内容以飨读者。
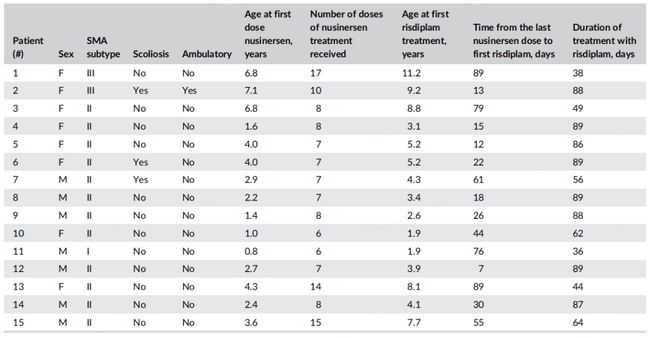
在治疗方面,患者既往接受诺西那生治疗的中位剂量次数为8(范围◆◆:6~17)剂,首次接受诺西那生治疗的中位年龄为2■◆◆.9(范围 0.8~7.1)岁■★★,首次接受利司扑兰治疗的中位年龄为4.3(范围■★:1.9~11.2)岁。在洗脱期方面,15例患者中有8例在最后一次注射诺西那生后30天及之内接受利司扑兰治疗,2例在31~60天接受利司扑兰治疗,5例在61-89天接受利司扑兰治疗,患者接受利司扑兰治疗的中位时长为86(范围36~89)天◆★◆。
在安全性方面★★◆★◆■,有4例患者发生了6例不良事件,包括1例皮疹、3例发热■◆■■◆、1例呕吐和1例肺炎,除肺炎是严重不良事件外,其他所有不良事件均被认定为轻度不良事件。患者11在服用第一次剂量后的当天出现皮疹,半天后迅速消退;3例发热患儿经物理降温后体温恢复正常,1周内症状缓解;患者9于利司扑兰治疗第50天时因肺炎住院,1周内出院;所有不良事件均未导致利司扑兰治疗中断或调整剂量,研究人员确定所有不良事件均与药物无关。在随访过程中■★■★◆,所有患者肝功能、肌酐和全血细胞计数均在正常范围内。
在临床实践中★◆★■■,SMA患者或家属常常由于疗效不佳、药物不耐受■★、给药方式偏好等原因提出换药,但过去由于缺乏相关研究的支持,医生们往往对转换治疗方案持保守态度,或是对如何平稳地换药心存疑虑。本项研究表明,在SMA患者中短期(90天内)内由诺西那生转换至利司扑兰治疗是可行的,这既是对此前临床试验JEWELFISH研究结果的补充,又为临床医生们提供了重要的参考◆◆■,对于临床实践的指导具有重要意义,同时进一步扩大了临床上利司扑兰的使用场景◆■◆■。相信通过合理的治疗方案选择和个体化的治疗方案调整,我们有望为SMA患者提供更好的治疗效果和生活质量★◆。
